2016年医疗器械监管工作报告.docx
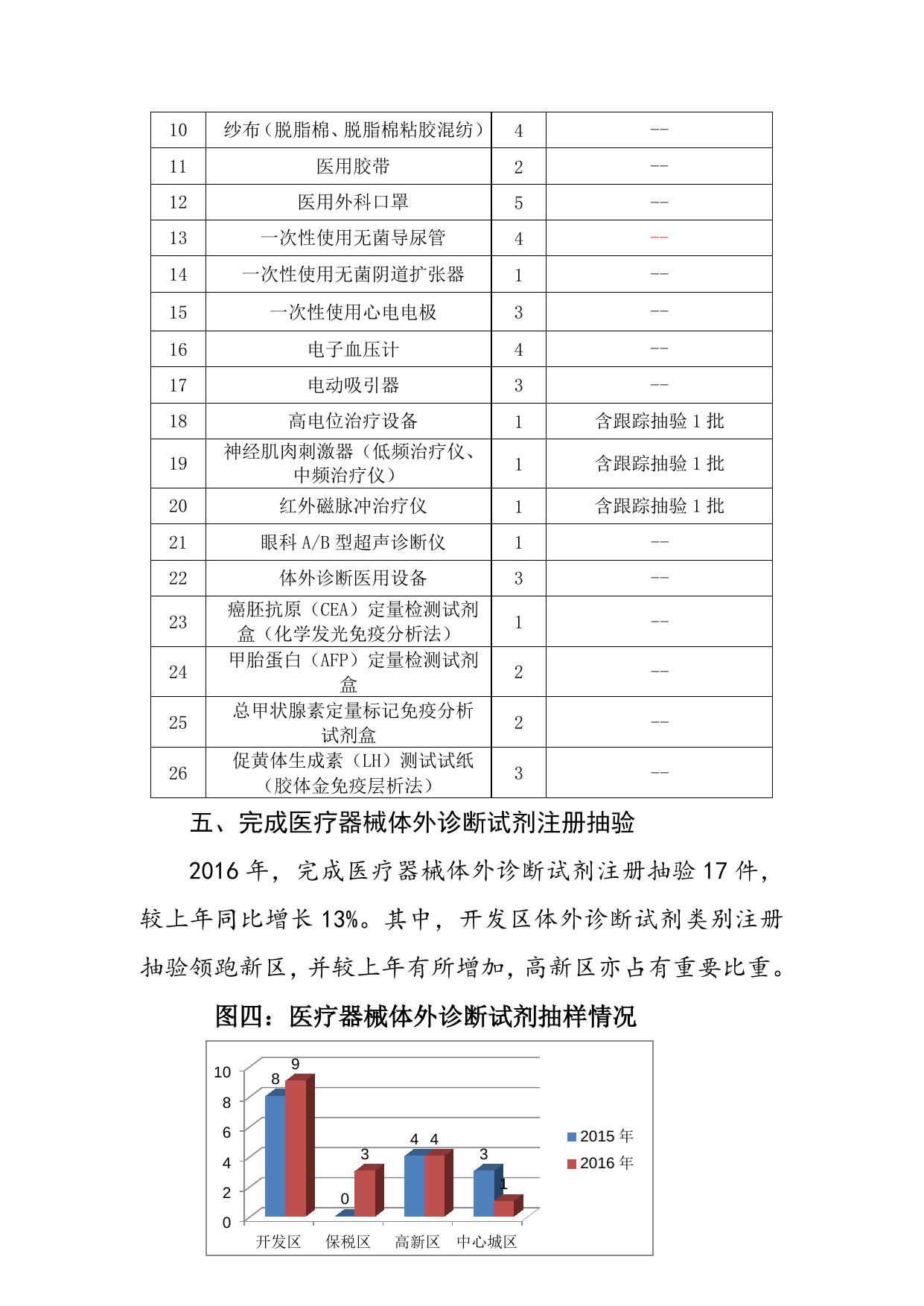
2016 年医疗器械监管工作报告 2016 年,新区市场监管局不断完善监管机制、拓展监管 方式、提高综合效能,推动医疗器械监管工作稳中求进,确 保人民群众用械安全,服务医疗器械行业健康发展。 一、滨海新区医疗器械产业概况 全区现有医疗器械生产、经营、使用单位共计 1822 家。 生产企业 147 家(其中三类生产企业 52 家),占全市总量的 37.4%;经营企业 600 家,占全市总量的 17.52%;使用单位 1075 家。医疗器械生产企业涵盖体外诊断试剂类、骨科植入 类、一次性无菌类、有源电气类等不同种类产品。 表一:医疗器械主要产品及代表企业 重点产品门类 代表企业 骨科植入 天津正天、威曼 介入产品 赛诺医疗 体外诊断设备及试剂 中新科炬 数字影像 天津邦盛医疗 医用高分子 哈娜好医材 高频仪器 中亚医疗、赛盟 眼科诊疗设备 索维电子、迈达 口腔类设备 杰冠 激光治疗设备 蓝莫德 二、开展医疗器械生产企业量化等级评定 2016 年,共有 106 家医疗器械生产企业参加量化等级评 定,均为二、三类医疗器械产品生产企业。综合评定结果为 A 级 16 家,B 级 81 家,C 级 9 家。较 2015 年参评生产企业 家数增加 26%,其中 B 级生产企业增加 32 家,D 级减少为零。 图一:2016 年医疗器械生产企业量化等级评定情况 9家 9% 16 家 15% 81 家 76% 全区已连续三年开展医疗器械生产企业量化等级评定 工作,并根据连续两年的评定结果为获得 A 级评定结果的企 业颁发放心医疗器械生产企业的牌匾。新区市场监管局根据 评定结果,对企业实行动态监管,对评级结果较差企业提高 监管频次,定期跟踪复查,有效保障医疗器械质量安全。 三、加强医疗器械不良事件监测 2016 年,共建设医疗器械不良事件监测哨点 169 家,其 中生产企业 119 个,经营企业 34 个,医疗机构 16 个。全年 完成医疗器械不良事件报告共计 363 例,较 2015 年完成数 量增加 13.8%。 图二:2014-2016 年医疗器械不良事件上报情况 2014-2016 不良事件上报情况 例 500 450 446 400 363 350 319 300 250 200 2014 2015 2016 年 四、加强医疗器械监督抽验 2016 年,完成国家质量监督抽验 42 个批次。完成天津 市监督抽验 77 个批次,涉及医疗器械生产、销售、使用各 环节。 表二:2016 年医疗器械监督抽样情况 序号 医疗器械抽验品种分配 批次 不合格产品跟踪抽验情况 1 一次性使用无菌注射器 2 -- 2 一次性使用输液器 3 含跟踪抽验 1 批 3 一次性使用穿刺针 4 -- 4 金属骨针 3 含跟踪抽验 1 批 5 宫内节育器 2 -- 6 非顺应性 PTCA 球囊扩张导管 1 -- 7 医用可吸收缝线 3 -- 8 医用防护口罩 1 -- 9 医用脱脂棉 5 -- 10 纱布(脱脂棉、脱脂棉粘胶混纺) 4 -- 11 医用胶带 2 -- 12 医用外科口罩 5 -- 13 一次性使用无菌导尿管 4 -- 14 一次性使用无菌阴道扩张器 1 -- 15 一次性使用心电电极 3 -- 16 电子血压计 4 -- 17 电动吸引器 3 -- 18 高电位治疗设备 1 含跟踪抽验 1 批 19 神经肌肉刺激器(低频治疗仪、 中频治疗仪) 1 含跟踪抽验 1 批 20 红外磁脉冲治疗仪 1 含跟踪抽验 1 批 21 眼科 A/B 型超声诊断仪 1 -- 22 体外诊断医用设备 3 -- 1 -- 2 -- 2 -- 3 -- 23 24 25 26 癌胚抗原(CEA)定量检测试剂 盒(化学发光免疫分析法) 甲胎蛋白(AFP)定量检测试剂 盒 总甲状腺素定量标记免疫分析 试剂盒 促黄体生成素(LH)测试试纸 (胶体金免疫层析法) 五、完成医疗器械体外诊断试剂注册抽验 2016 年,完成医疗器械体外诊断试剂注册抽验 17 件, 较上年同比增长 13%。其中,开发区体外诊断试剂类别注册 抽验领跑新区,并较上年有所增加,高新区亦占有重要比重。 图四:医疗器械体外诊断试剂抽样情况 10 8 9 8 6 3 4 2 0 4 4 2015 年 3 2016 年 1 0 开发区 保税区 高新区 中心城区 六、高风险医疗器械生产企业监管 2016 年,新区市场监管局继续在高风险医疗器械生产企 业监管中推广第三方监管模式,共对 38 家高风险企业进行 检查,主要涉及无菌、植入性医疗器械产品。重点检查人员 资质及培训、设备维护监测、原材料采购及检测、生产工艺 规程及生产记录、生产环境控制等方面,坚决治理原材料不 合规、用水制备不合规、擅自变更生产工艺等行为。 累计查找到 331 个缺陷项,涉嫌违法行为 69 项。针对 发现问题,新区市场监管局及时进行了通报,并根据检查结 果对相关当事人依法严肃处理。同时,联合第三方专业机构, 对全部医疗器械生产企业深入开展宣传教育,分析讲解共性 问题,提出整改落实方案,切实推动企业履行主体责任,改 进生产管理规范,取得良好反响。

 2016年医疗器械监管工作报告.docx
2016年医疗器械监管工作报告.docx